.
NAMA : EMILIA NAFAZA
NPM : 2013023002
Izin bertanya, Bagaimanakah kelemahan dan kelebihan dari Teori Asam Basa Usanovich?
NPM : 2013023002
Izin bertanya, Bagaimanakah kelemahan dan kelebihan dari Teori Asam Basa Usanovich?
Nama: Ayu Febrina Mutiara Ad'ha
NPM: 2013023062
Izin menjawab pertanyaan emil,
Kelebihan Teori Usanovich diantaranya:
Memperluas teori asam basa menurut Lewis, sehingga senyawa yang belum diidentifikasi menurut Lewis bisa diidentifikasi melalui teori asam basa Usanovich.
sedangkan Kekurangan Teori Usanovich:
Teori asam basa ini tidak diakui dunia atau dibilang bukan teorinya, disebabkan teori yang diungkapkan Usanovich merupakan gabungan dari semua teori asam basa yang pernah diungkapkan oleh ahli kimia yang lain.
Kelebihan Teori Usanovich diantaranya:
Memperluas teori asam basa menurut Lewis, sehingga senyawa yang belum diidentifikasi menurut Lewis bisa diidentifikasi melalui teori asam basa Usanovich.
sedangkan Kekurangan Teori Usanovich:
Teori asam basa ini tidak diakui dunia atau dibilang bukan teorinya, disebabkan teori yang diungkapkan Usanovich merupakan gabungan dari semua teori asam basa yang pernah diungkapkan oleh ahli kimia yang lain.
Dapat dikatan definisi Usanovich ini telah mencakup semua definisi yang telah ada sebelumnya.
Nama : Mulyawan Saputra
npm : 2013023038
izin bertanya mengapa person dapat mengatakan ion-ion yang memiliki muatan densitas yang besar bersifat keras?
npm : 2013023038
izin bertanya mengapa person dapat mengatakan ion-ion yang memiliki muatan densitas yang besar bersifat keras?
Nama : Artika Rahmadana
Kelas : 3B
NPM : 2013023026
Izin menjawab pertanyaaan mulyawan saputra, Ion-ion yang memiliki densitas muatan yang besar umumnya memiliki ukura kecil dan sukar dipolarisasi. Oleh karena sulit terpolarisasi maka dikatakan oleh pearson ion-ion dengan densitas yang besar dan dan susah terpolarisasi itu bersifat keras.
Kelas : 3B
NPM : 2013023026
Izin menjawab pertanyaaan mulyawan saputra, Ion-ion yang memiliki densitas muatan yang besar umumnya memiliki ukura kecil dan sukar dipolarisasi. Oleh karena sulit terpolarisasi maka dikatakan oleh pearson ion-ion dengan densitas yang besar dan dan susah terpolarisasi itu bersifat keras.
Nama : Zhilal Zhafirah
NPM 2013023034
Izin bertanya,
Bagaimanakah kekuatan asam-asam oksi?
NPM 2013023034
Izin bertanya,
Bagaimanakah kekuatan asam-asam oksi?
Nama: Ayu Febrina Mutiara Ad'ha
NPM: 2013023062
Izin menjawab pertanyaan dari zilal,
ada dua faktor yang dapat digunakan memprediksi apakah suatu asam atau basa tergolong asam kuat atau basa kuat, yaitu:
1. ditinjau dari keelektronegatifan atom pusat asam
2. kestabilan anion (basa konjugasinya) setelah asam tersebut melepaskan proton. Semakin stabil anion sisa asamnya maka asam tersebut semakin kuat. Bila basa konjugasi tidak stabil maka ia dapat bereaksi balik dengan H+ membentuk asam semula.
untuk memudahkan perkiraan kekuatan asam kita dapat melihat selisih jumlah H dan O dalam asam-asam oksi (asam yang mengandung O). Semakin sedikit selisih H dan O maka sifat asamnya semakin lemah, sebaliknya semakin banyak selisih H dan O maka sifat asamnya semakin kuat.
NPM: 2013023062
Izin menjawab pertanyaan dari zilal,
ada dua faktor yang dapat digunakan memprediksi apakah suatu asam atau basa tergolong asam kuat atau basa kuat, yaitu:
1. ditinjau dari keelektronegatifan atom pusat asam
2. kestabilan anion (basa konjugasinya) setelah asam tersebut melepaskan proton. Semakin stabil anion sisa asamnya maka asam tersebut semakin kuat. Bila basa konjugasi tidak stabil maka ia dapat bereaksi balik dengan H+ membentuk asam semula.
untuk memudahkan perkiraan kekuatan asam kita dapat melihat selisih jumlah H dan O dalam asam-asam oksi (asam yang mengandung O). Semakin sedikit selisih H dan O maka sifat asamnya semakin lemah, sebaliknya semakin banyak selisih H dan O maka sifat asamnya semakin kuat.
Nama : NENGAH ANGGI PUSPA DEWI
NPM : 2013023058
Izin bertanya, apa yang dimaksud dengan asam terner dan apakah semua senyawa asam masuk dalam senyawa asam terner?
NPM : 2013023058
Izin bertanya, apa yang dimaksud dengan asam terner dan apakah semua senyawa asam masuk dalam senyawa asam terner?
Sebagai balasan Nengah Anggi Puspa Dewi 2013023058
Re: ASam-Basa anorganik
oleh Justine 2013023024 -
Nama : Justine
NPM : 2013023024
Izin menjawab pertanyaan Nengah Anggi
Asam terner merupakan senyawa asam yang tersusun dari tiga jenis unsur yang berbeda. semua senyawa asam belum tentu senyawa terner karena masih ada senyawa asam yang merupakan senyawa biner dan senyawa quarterner.
NPM : 2013023024
Izin menjawab pertanyaan Nengah Anggi
Asam terner merupakan senyawa asam yang tersusun dari tiga jenis unsur yang berbeda. semua senyawa asam belum tentu senyawa terner karena masih ada senyawa asam yang merupakan senyawa biner dan senyawa quarterner.
Nama : Annisa Sholeha
NPM : 2013023032
izin bertanya, apa saja contoh pelarut sangat polar dan berautodisosiasi?
NPM : 2013023032
izin bertanya, apa saja contoh pelarut sangat polar dan berautodisosiasi?
Nama : Justine
NPM : 2013023024
izin menjawab pertanyaan annisa sholeha
Pelarut sangat polar dan berautodisosiasi

NAMA : ALVINA MIRANDA
NPM : 2013023016
Izin bertanya, Bagaimana asam - basa menurut usanovich?
NPM : 2013023016
Izin bertanya, Bagaimana asam - basa menurut usanovich?
Nama : Justine
NPM : 2013023024
Izin menjawab pertanyaan Alvina Miranda
Asam menurut Usanovich adalah setiap spesi kimia yang bereaksi dengan basa, menyerahkan kation dan menerima anion (elektron), sedangkan basa adalah setiap spesi kimia yang bereaksi dengan asam, menyerahkan anion (elektron) atau menerima kation.
NPM : 2013023024
Izin menjawab pertanyaan Alvina Miranda
Asam menurut Usanovich adalah setiap spesi kimia yang bereaksi dengan basa, menyerahkan kation dan menerima anion (elektron), sedangkan basa adalah setiap spesi kimia yang bereaksi dengan asam, menyerahkan anion (elektron) atau menerima kation.
Nama : Dewi Shinta Amelia
NPM : 2013023052
Izin bertanya, apa yang membedakan asam keras, daerah antara (borderline), dan asam lunak?
NPM : 2013023052
Izin bertanya, apa yang membedakan asam keras, daerah antara (borderline), dan asam lunak?
Nama: Ayu Febrina Mutiara Ad'ha
NPM: 20130230632
Izin menjawab pertanyaan dewi,
asam keras adalah ion logam-logam yang terletak pada bagian kiri sistem periodik unsur, peristiwa ini paralel dengan rendahnya sifat elektronegatif atau tingginya sifat elektropositif logam-logam yang bersangkutan.
Daerah batas umumnya terdapat pada logam-logam transisi.Golongan utama logam pada bagian kanan sistem periodik unsur bersifat asam lunak.
NPM: 20130230632
Izin menjawab pertanyaan dewi,
asam keras adalah ion logam-logam yang terletak pada bagian kiri sistem periodik unsur, peristiwa ini paralel dengan rendahnya sifat elektronegatif atau tingginya sifat elektropositif logam-logam yang bersangkutan.
Daerah batas umumnya terdapat pada logam-logam transisi.Golongan utama logam pada bagian kanan sistem periodik unsur bersifat asam lunak.
Sifat asam juga berkaitan dengan muatan ion; beberapa ion logam tertentu bersifat aman lunak bagi muatan ion rendah dan keras bagi muatan ion ton tinggi.
Nama: Apriza Yanti
NPM: 2013023064
Izin bertanya,
Bagaimana asam-basa dalam sistem pelarut?
NPM: 2013023064
Izin bertanya,
Bagaimana asam-basa dalam sistem pelarut?
Nama : Justine
NPM : 2013023024
izin menjawab pertanyaan apriza
Dalam sistem pelarut asam adalah zat-zat yang menaikkan konsentrasi kation spesifik pelarut dan sistem pelarut basa adalah zat-zat yang menaikkan konsentrasi anion spesifik pelarut.
NPM : 2013023024
izin menjawab pertanyaan apriza
Dalam sistem pelarut asam adalah zat-zat yang menaikkan konsentrasi kation spesifik pelarut dan sistem pelarut basa adalah zat-zat yang menaikkan konsentrasi anion spesifik pelarut.
Nama : Rizka Awalia Rodhiah
Npm : 2013023060
Izin bertanya,
Faktor faktor apa sajakah yang mempengaruhi asam asam oksi?
Npm : 2013023060
Izin bertanya,
Faktor faktor apa sajakah yang mempengaruhi asam asam oksi?
Nama : Artika Rahmadana
Kelas : 3B
NPM : 2013023026
Izin menjawab pertanyaan dari rizka awalia rodhiah, faktor yang mempengaruhi kekuatan asam oksi adalah:
1. Pengaruh muatan formal
2. Pengaruh ikatan X
3. Signifikansi orbital d
4. Pengaruh Solvasi
Kelas : 3B
NPM : 2013023026
Izin menjawab pertanyaan dari rizka awalia rodhiah, faktor yang mempengaruhi kekuatan asam oksi adalah:
1. Pengaruh muatan formal
2. Pengaruh ikatan X
3. Signifikansi orbital d
4. Pengaruh Solvasi
Nama : Nurul Hidayah
NPM. : 2013023022
Izin bertanya, pada tahun 1939 Usanovich mengenalkan klasifikasi asam-basa nya, namun mengapa definisi asam-basa Usanovish ditolak oleh para kimiawan?
NPM. : 2013023022
Izin bertanya, pada tahun 1939 Usanovich mengenalkan klasifikasi asam-basa nya, namun mengapa definisi asam-basa Usanovish ditolak oleh para kimiawan?
Nama : Justine
NPM : 2013023024
Izin menjawab pertanyaan Nurul hidayah
Definisi asam basa menurut usanovich dikembangkan berdasarkan asam basa Lewis dengan memasukkan oksidator ( menerima elektron dari sistem) sebagai asam dan reduktor (memberikan elektron ke sistem) sebagai basa. Dari definisi tersebut secara eksplisit reaksi redoks juga merupakan reaksi asam-basa. Akan tetapi reaksi asam-basa belum tentu merupakan reaksi redoks. Selain itu juga, definisi tersebut telah mencakup baik semua definisi asam basa yang telah ada sebelumnya maupun reaksi reduksi oksidasi sebagai kelas khusus dalam reaksi asam- basa. Karena hal yang demikian definisi asam basa menurut usanovich ditolak oleh para kimiawan pada saat itu.
NPM : 2013023024
Izin menjawab pertanyaan Nurul hidayah
Definisi asam basa menurut usanovich dikembangkan berdasarkan asam basa Lewis dengan memasukkan oksidator ( menerima elektron dari sistem) sebagai asam dan reduktor (memberikan elektron ke sistem) sebagai basa. Dari definisi tersebut secara eksplisit reaksi redoks juga merupakan reaksi asam-basa. Akan tetapi reaksi asam-basa belum tentu merupakan reaksi redoks. Selain itu juga, definisi tersebut telah mencakup baik semua definisi asam basa yang telah ada sebelumnya maupun reaksi reduksi oksidasi sebagai kelas khusus dalam reaksi asam- basa. Karena hal yang demikian definisi asam basa menurut usanovich ditolak oleh para kimiawan pada saat itu.
Nama : Ika Diva Agustin
Npm: 2013023004
Izin bertanya Apa saja kelebihan dan kekurangan dari asam-basa Luc-Flood?
Npm: 2013023004
Izin bertanya Apa saja kelebihan dan kekurangan dari asam-basa Luc-Flood?
Nama : Justine
NPM : 2013023024
Izin menjawab pertanyaan Ika Diva
Pada teori Lux-Flood ini memiliki kekurangan dan kelebihan masing-masing. Untuk kekurangannya teori asam-basa Lux-Flood terbatas pada sistem lelehan oksida. Sedangkan kelebihannya karakterisasi oksida logam dan nonlogam menggunakan sistem ini bermanfaat dalam industri pembuatan logam.
NPM : 2013023024
Izin menjawab pertanyaan Ika Diva
Pada teori Lux-Flood ini memiliki kekurangan dan kelebihan masing-masing. Untuk kekurangannya teori asam-basa Lux-Flood terbatas pada sistem lelehan oksida. Sedangkan kelebihannya karakterisasi oksida logam dan nonlogam menggunakan sistem ini bermanfaat dalam industri pembuatan logam.
NAMA: ERVIANTINA H
NPM: 2013023036
izin bertanya, "menurut Pearson dalam senyawa kompleks berdasarkan kereaktivannya terhadap ligan..."
lalu apa yang dimaksud dengan ligan?
NPM: 2013023036
izin bertanya, "menurut Pearson dalam senyawa kompleks berdasarkan kereaktivannya terhadap ligan..."
lalu apa yang dimaksud dengan ligan?
Nama : Justine
NPM : 2013023024
Izin menjawab pertanyaan Erviantina
Ligan adalah sebuah ion atau molekul netral yang mampu mengikat secara koordinasi atom atau ion logam pusat dalam senyawa kompleks. Molekul ini berperan sebagai basa Lewis (donor pasangan elektron), dan logam pusat yang mengikatnya berperan sebagai asam Lewis (akseptor pasangan elektron).
NPM : 2013023024
Izin menjawab pertanyaan Erviantina
Ligan adalah sebuah ion atau molekul netral yang mampu mengikat secara koordinasi atom atau ion logam pusat dalam senyawa kompleks. Molekul ini berperan sebagai basa Lewis (donor pasangan elektron), dan logam pusat yang mengikatnya berperan sebagai asam Lewis (akseptor pasangan elektron).
Sebagai balasan Noor Fadiawati
Re: ASam-Basa anorganik
Nama : Elisabet Erlian Nadia Putri
NPM : 2013023042
Izin bertanya, Bagaimana syarat asam-basa keras dan asam basa lunak?
NPM : 2013023042
Izin bertanya, Bagaimana syarat asam-basa keras dan asam basa lunak?
Sebagai balasan Elisabet Erlian Nadia Putri 2013023042
Re: ASam-Basa anorganik
oleh Ayu Febrina Mutiara Ad'ha -
Nama: Ayu Febrina Mutiara ad'ha
NPM: 2013023062
izin menjawab pertanyaan dari elisabet,
syarat syarat asam basa keras, yaitu:
1. jari jari aton kecil
2. bilangan oksidasinya tinggi
3. polaritasnya rendah
4. elektronegatifitasnya tinggi.
sedangkan syarat syarat asam basa lunak, yaitu:
1. jari jari atom besar
2. bilangan oksidasinya item
3. polaritasnya tinggi
4. elektronegatifitasnya rendah
NPM: 2013023062
izin menjawab pertanyaan dari elisabet,
syarat syarat asam basa keras, yaitu:
1. jari jari aton kecil
2. bilangan oksidasinya tinggi
3. polaritasnya rendah
4. elektronegatifitasnya tinggi.
sedangkan syarat syarat asam basa lunak, yaitu:
1. jari jari atom besar
2. bilangan oksidasinya item
3. polaritasnya tinggi
4. elektronegatifitasnya rendah
Nama : Adelia Putri
NPM : 2013023014
Izin bertanya
Dijelaskan bahwa asam keras cenderung menyukai basa keras dan sebaliknya, asam lunak cenderung menyukai basa lunak. Mengapa demikian?
NPM : 2013023014
Izin bertanya
Dijelaskan bahwa asam keras cenderung menyukai basa keras dan sebaliknya, asam lunak cenderung menyukai basa lunak. Mengapa demikian?
Nama : Artika Rahmadana
NPM : 2013023026
Izin menjawab pertanyaan Adelia Putri, Asam keras cenderung lebih suka untuk berkoordinasi dengan basa keras, dan demikian juga halnya dengan asam lunak yang cenderung lebih suka berkoordinasi dengan basa lunak. Asam keras dan basa keras cenderung mempunyai atom yang kecil, oksidasi tinggi, kepolaran rendah, dan keelektronegatifan tinggi. Sedangkan asam dan basa lunak cenderung mempunyai atom yang besar, tingkat oksidasi rendah, dan elektronegatifan rendah.
Pada kenyataannya asam keras yang berikatan dengan dengan basa keras akan memiliki kestabilan yang lebih tinggi dibandingkan asam keras yang berikatan dengan basa lunak. Asam keras (misalnya : Fe3+) yang berikatan dengan halogen, kestabilannya akan menurun berdasarkan urutan : F- > Cl- > Br- > I-. Sedangkan asam lunak (misalnya : Hg2+) yang berikatan dengan golongan halogen, kestabilannya akan meningkat berdasarkan urutan : F- < Cl- < Br- < I-. Hal ini disebabkan karena F- dan Cl- merupakan basa keras, sehingga akan lebih stabil jika berikatan dengan asam keras, sebaliknya I‑ yang merupakan basa lunak, akan lebih stabil jika berikatan dengan asam lunak.
NPM : 2013023026
Izin menjawab pertanyaan Adelia Putri, Asam keras cenderung lebih suka untuk berkoordinasi dengan basa keras, dan demikian juga halnya dengan asam lunak yang cenderung lebih suka berkoordinasi dengan basa lunak. Asam keras dan basa keras cenderung mempunyai atom yang kecil, oksidasi tinggi, kepolaran rendah, dan keelektronegatifan tinggi. Sedangkan asam dan basa lunak cenderung mempunyai atom yang besar, tingkat oksidasi rendah, dan elektronegatifan rendah.
Pada kenyataannya asam keras yang berikatan dengan dengan basa keras akan memiliki kestabilan yang lebih tinggi dibandingkan asam keras yang berikatan dengan basa lunak. Asam keras (misalnya : Fe3+) yang berikatan dengan halogen, kestabilannya akan menurun berdasarkan urutan : F- > Cl- > Br- > I-. Sedangkan asam lunak (misalnya : Hg2+) yang berikatan dengan golongan halogen, kestabilannya akan meningkat berdasarkan urutan : F- < Cl- < Br- < I-. Hal ini disebabkan karena F- dan Cl- merupakan basa keras, sehingga akan lebih stabil jika berikatan dengan asam keras, sebaliknya I‑ yang merupakan basa lunak, akan lebih stabil jika berikatan dengan asam lunak.
Nama: Anisa Auliya Sapitri
Npm: 2013023020
Izin bertanya kepada kelompok 12, kan sudah dijelaskan terkait asam oksi di antaranya penamaan asam-asam oksi dan struktur asam-asam oksi. Pertanyaan saya bagaimana penjelasan dari asam asam oksi tersebut?
Npm: 2013023020
Izin bertanya kepada kelompok 12, kan sudah dijelaskan terkait asam oksi di antaranya penamaan asam-asam oksi dan struktur asam-asam oksi. Pertanyaan saya bagaimana penjelasan dari asam asam oksi tersebut?
Sebagai balasan Anisa Auliya Sapitri 2013023020
Re: ASam-Basa anorganik
oleh Ayu Febrina Mutiara Ad'ha -
Nama: Ayu Febrina Mutiara Ad'ha
NPM: 2013023062
izin menjawab pertanyaan dari anisa auliya sapitri
Asam oksi artinya asam anorganik yang menandung oksigen atau asam asam anorganik
Secara khusus, itu adalah senyawa yang mengandung hidrogen, oksigen, dan setidaknya satu elemen lainnya, dengan setidaknya satu ikatan atom hidrogen ke oksigen yang dapat berdisosiasi untuk menghasilkan kation dan anion asam.
NPM: 2013023062
izin menjawab pertanyaan dari anisa auliya sapitri
Asam oksi artinya asam anorganik yang menandung oksigen atau asam asam anorganik
Secara khusus, itu adalah senyawa yang mengandung hidrogen, oksigen, dan setidaknya satu elemen lainnya, dengan setidaknya satu ikatan atom hidrogen ke oksigen yang dapat berdisosiasi untuk menghasilkan kation dan anion asam.
Nama : Upit Nurjanah
Npm : 2013023050
Izin bertanya, terkait asam-asam oksi, asam-asam oksi terdiri dari berapa jenis?
Npm : 2013023050
Izin bertanya, terkait asam-asam oksi, asam-asam oksi terdiri dari berapa jenis?
Nama : Artika Rahmadana
NPM : 2013023026
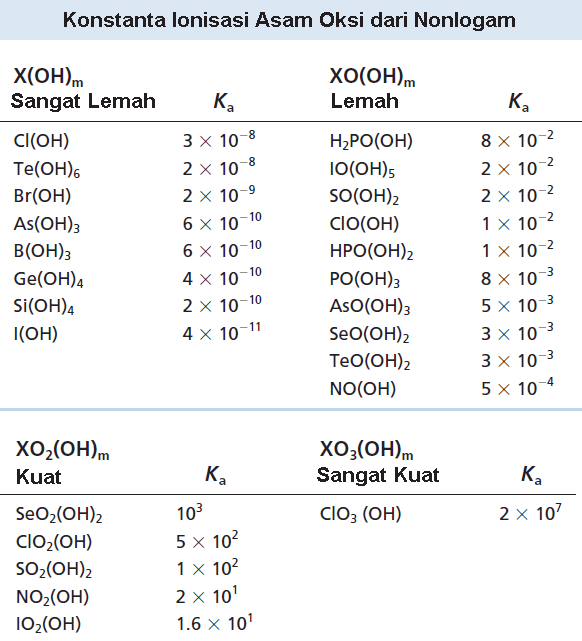
Izin menjawab, Asam oksi di sini dikelompokkan menjadi 4 jenis dengan rumus umum:
X(OH)m, contohnya Cl(OH) atau HClO
XO(OH)m, contohnya PO(OH)3 atau OP(OH)3 atau H3PO4
XO2(OH)m, contohnya SO2(OH)2 atau O2S(OH)2 atau H2SO4
XO3(OH)m, contohnya ClO3(OH) atau O3Cl(OH) atau HClO4
Secara umum pada jenis senyawa oksi seperti di atas ini H selalu berikatan dengan atom O dan tidak pernah berikatan dengan atom pusat secara langsung. Untuk rumus asam oksi lain bila jumlah H lebih banyak (atau kadang sama) dari jumlah O maka H berkemungkinan (berpeluang) untuk berikatan langsung dengan atom pusat.
NPM : 2013023026
Izin menjawab, Asam oksi di sini dikelompokkan menjadi 4 jenis dengan rumus umum:
X(OH)m, contohnya Cl(OH) atau HClO
XO(OH)m, contohnya PO(OH)3 atau OP(OH)3 atau H3PO4
XO2(OH)m, contohnya SO2(OH)2 atau O2S(OH)2 atau H2SO4
XO3(OH)m, contohnya ClO3(OH) atau O3Cl(OH) atau HClO4
Secara umum pada jenis senyawa oksi seperti di atas ini H selalu berikatan dengan atom O dan tidak pernah berikatan dengan atom pusat secara langsung. Untuk rumus asam oksi lain bila jumlah H lebih banyak (atau kadang sama) dari jumlah O maka H berkemungkinan (berpeluang) untuk berikatan langsung dengan atom pusat.
